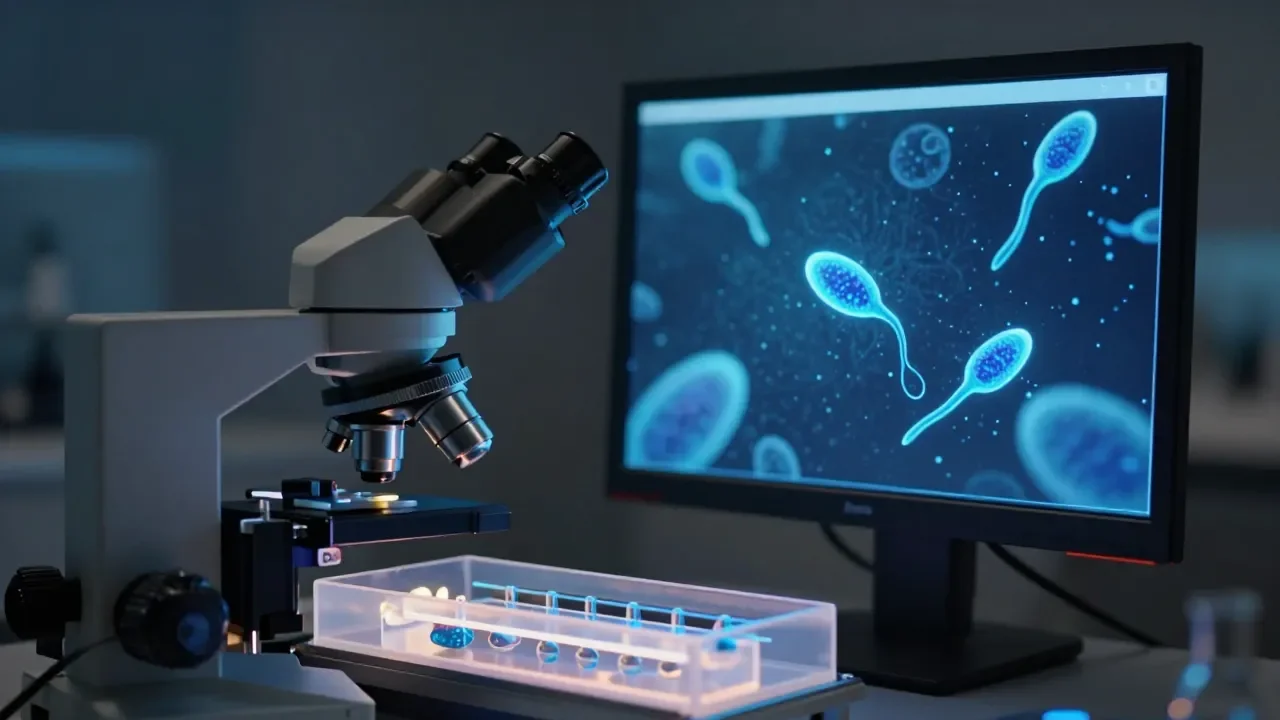
Um sistema baseado em inteligência artificial desenvolvido pela Universidade de Columbia, nos Estados Unidos, está conseguindo localizar espermatozoides em homens diagnosticados como azoospérmicos — ou seja, que não apresentam espermatozoides detectáveis no líquido ejaculado. A tecnologia, chamada Star (sigla em inglês para Rastreamento e Recuperação de Espermatozoides), já permitiu o nascimento de pelo menos um bebê e está em uso regular no centro de fertilidade da universidade, com uma lista de espera que reúne centenas de pacientes de diferentes países.
A azoospermia afeta cerca de 1% de todos os homens e está presente em aproximadamente 10% dos casos de infertilidade masculina. A condição pode ser causada por diversos fatores, entre eles a síndrome de Klinefelter, um distúrbio genético em que homens nascem com um cromossomo X extra. A maioria dos portadores produz pouco ou nenhum espermatozoide no líquido ejaculado, e o diagnóstico frequentemente só ocorre na fase adulta, quando o casal já enfrenta dificuldades para conceber.

A infertilidade é um problema global: cerca de uma em cada seis pessoas em idade reprodutiva enfrenta dificuldades para engravidar pelo menos uma vez na vida, e a infertilidade masculina contribui em até metade dos casos. Para esses homens, cujas amostras podem conter apenas um único espermatozoide entre milhões de detritos celulares, a busca manual ao microscópio é praticamente inviável.
O diretor do Centro de Fertilidade da Universidade de Columbia, Zev Williams, teve a inspiração para o sistema Star em 2020, ao ler sobre o uso de algoritmos de aprendizado de máquina para identificar novas estrelas em imagens de telescópios. Ele percebeu uma semelhança entre o desafio dos astrônomos — encontrar objetos raros em meio a uma quantidade colossal de dados — e o dos embriologistas que tentam localizar um espermatozoide em amostras consideradas vazias.
A tecnologia combina chips microfluídicos, dispositivos de vidro ou polímero gravados com canais tão finos quanto um fio de cabelo, com um sistema de imagem de alta resolução capaz de capturar 300 imagens por segundo enquanto a amostra flui pelos canais. Um algoritmo de aprendizado de máquina analisa essas imagens em tempo real, distinguindo espermatozoides dos detritos e fragmentos celulares que compõem a maior parte do material examinado.
Quando um espermatozoide é detectado, um sistema robótico entra em ação em milissegundos, separando a fração do fluido que contém a célula identificada. O resultado é uma pequena gota concentrada com os espermatozoides recuperados, prontos para serem utilizados em procedimentos de fertilização in vitro. Williams afirma que o sistema atingiu uma taxa de sensibilidade de 100%, ou seja, é capaz de encontrar um único espermatozoide presente na amostra.
Nos testes realizados pela equipe, o Star encontrou 40 vezes mais espermatozoides do que a busca manual feita por um técnico treinado. Entre os últimos 175 pacientes que passaram pelo sistema — todos previamente informados de que não teriam chance de ter filhos biológicos —, espermatozoides foram localizados em pouco menos de 30% dos casos.
O primeiro bebê nascido com a ajuda da tecnologia Star veio ao mundo no final de 2025, após cinco anos de desenvolvimento do sistema. O casal havia lidado com infertilidade por quase duas décadas. Williams relata que a equipe comemorou intensamente a conquista, ressaltando que poucos resultados na carreira de um pesquisador têm uma recompensa tão significativa.
O caso do casal formado por Penelope e Samuel — cujos nomes foram alterados para preservar a identidade — ilustra o funcionamento do sistema em uma situação especialmente complexa. Samuel foi diagnosticado com síndrome de Klinefelter e informado de que tinha apenas 20% de chance de ter um filho biológico. Ele passou por nove meses de terapia hormonal antes de se submeter a uma cirurgia de extração de tecido testicular em outro centro de fertilidade.
O material coletado foi encaminhado ao laboratório da Universidade de Columbia, onde Eric Forman, diretor médico e de laboratório do centro, supervisionou o processamento. Ao mesmo tempo, Penelope realizava a coleta de óvulos, e a equipe trabalhava contra o relógio, já que amostras frescas oferecem melhores taxas de fertilização. O sistema Star isolou oito espermatozoides da amostra de Samuel, que foram injetados nos óvulos de Penelope. Apenas um se desenvolveu até o estágio de blastocisto, um embrião em fase mais avançada, mas foi suficiente: Penelope está grávida, com o bebê previsto para o final de julho.
Para o casal, a gravidez representa o fim de dois anos e meio de tentativas, exames e frustrações. Samuel conta que, ao saber do diagnóstico, temia não conseguir realizar o sonho de ter um filho biológico. Penelope descreve o momento em que compartilhou a notícia com o marido como uma explosão de emoção, com lágrimas diante da constatação de que todo o esforço havia valido a pena.
A aplicação da inteligência artificial na medicina reprodutiva não se limita à busca de espermatozoides. Na estimulação ovariana, etapa essencial da fertilização in vitro em que os ovários são estimulados a produzir múltiplos óvulos, algoritmos de aprendizado de máquina já permitem o cálculo personalizado de dosagens hormonais. Ferramentas de aprendizado profundo também vêm sendo empregadas para selecionar com mais precisão os gametas e embriões mais viáveis.
Especialistas ouvidos pela reportagem, no entanto, alertam para a necessidade de cautela. Siobhan Quenby, professora de obstetrícia da Universidade de Warwick, no Reino Unido, reconhece que a combinação de tecnologia avançada, engenharia e inteligência artificial oferece uma solução promissora para casos graves de subfertilidade masculina. Mas ressalta que uma gravidez bem-sucedida é apenas um começo, e que mais pesquisas com um número maior de pacientes são necessárias antes que o real valor do tratamento possa ser plenamente avaliado.
Quenby também chama a atenção para a vulnerabilidade de casais que enfrentam longas jornadas de tratamento de fertilidade, muitas vezes dispostos a investir em procedimentos caros e de eficácia não comprovada. A promessa exagerada de resultados positivos, segundo ela, é um risco que acompanha qualquer inovação nesse campo. Além disso, questões como o tratamento de dados médicos sensíveis, a confidencialidade das informações e a definição de responsabilidades em caso de falhas ainda exigem regulamentação mais clara.
Para Samuel, no entanto, a experiência mudou a perspectiva da família. O casal já pensa na possibilidade de ter um segundo filho, embora saiba que precisará passar pelo processo novamente, já que não há reservas de material congelado. A diferença agora, ele diz, é que onde antes não havia esperança, passou a existir uma possibilidade concreta.